El atomo gramo, es el peso en átomos de un mol de átomos (6,022 x 1023 átomos) de un elemento. Este peso es exactamente igual al peso atómico expresado en gramos.
1 At - g = P.A. g
Para realizar cálculos, tendremos que usar la siguiente relación:
Ejemplo 1:
Calcular el peso de un átomo de carbono en gramos. Dato: P.A. (C) = 12 uma
Solución:
Según la relación:
1 At-g (C) = 12 g (C) → 6,022 x 1023 átomos de (C)
Vemos que: 6,022 x 1023 átomos de (C) pesa 12 gramos.
Tenemos que calcular cuanto pesa 1 átomo de (C).
Aplicando una regla de tres simple:
X = 12 / 6,022 x 1023 = 2 x 10-23 gramos
Ejemplo 2:
Calcular el peso de un átomo de azufre en gramos. Dato: P.A. (S) = 32 uma
Solución:
Según la relación:
1 At-g (S) = 32 g (S) → 6,022 x 1023 átomos de (S)
Vemos que: 6,022 x 1023 átomos de (S) pesa 32 gramos.
Tenemos que calcular cuanto pesa 1 átomo de (S).
Aplicando una regla de tres simple:
X = 32 / 6,022 x 1023 = 5 x 10-23 gramos
Ejemplo 3:
Calcular el peso de un átomo de oxígeno en gramos. Dato: P.A. (O) = 16 uma
Respuesta: 2,7 x 10-23 gramos.
Ejemplo 4:
Calcular el peso de un átomo de Silicio en gramos. Dato: P.A. (Si) = 38 uma
Respuesta: 6,3 x 10-23 gramos.
Ejemplo 5:
Calcular el peso de un átomo de sodio en gramos. Dato: P.A. (Na) = 23 uma
Respuesta: 3,8 x 10-23 gramos.
Ejemplo 6:
Una medalla de plata pesa 10,8 gramos. ¿Cuántos átomos de plata contiene la medalla?. Dato P.A. (Ag) = 108 uma.
Solución:
Según la relación:
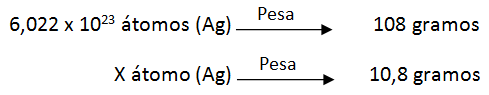
1 At-g (Ag) = 108 g (Ag) → 6,022 x 1023 átomos de (Ag)
Vemos que: 6,022 x 1023 átomos de (Ag) pesa 108 gramos.
Tenemos que calcular cuantos átomos hay en 10,8 gramos de plata (Ag)
Aplicando una regla de tres simple:
X = 6,022 x 1023 x 10,8 / 108
X = 6,022 x 1022 átomos de Ag
Ejemplo 7:
Una medalla de cobre pesa 635 gramos. ¿Cuántos átomos de cobre contiene la medalla?. Dato P.A. (Cu) = 63,5 uma.
Solución: 10 x 6,022 x 1023 = 6,022 x 1024
Ejemplo 8:
Una medalla de oro pesa 591 gramos. ¿Cuántos átomos de oro contiene la medalla?. Dato P.A. (Au) = 197 uma.
Solución: 3 x 6,022 x 1023
Ejemplo 9:
Se tiene una muestra de 200 gramos de Calcio (Ca). ¿cuántos atomos gramo contiene?. Dato P.A. (Ca) = 40 uma.
Solución:
1 At-g (Ca) = 40 g (Ca) → 6,022 x 1023 átomos de (Ca)
Vemos que: 1 At-g (Ca) contiene 40 gramos de átomos de (Ca)
Tenemos que calcular cuantos At-g hay en 200 gramos de calcio (Ca)
Aplicando una regla de tres simple:
X = 200 / 40 = 5 at-g
Ejemplo 10:
Se tiene una muestra de 156 gramos de Cromo (Cr). ¿cuántos atomos gramo contiene?. Dato P.A. (Cr) = 52 uma.
Solución: 3 at-g
Ejemplo 11:
Se tiene una muestra de 151 gramos de Fósforo (P). ¿cuántos atomos gramo contiene?. Dato P.A. (P) = 31 uma.
Solución: 5 at-g
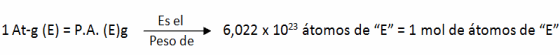
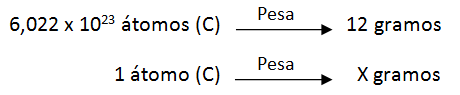


5 comentarios
muchas gracias!
muchas gracias me sirve bastante!!!
muy bueno aprendi mucho thanks
la definicion del atomo grama Ud. ha dado mal al decir: Es el peso en atomo de un mol de .... por favor?
El cobre natural está formado por los isotopos 63Cu y 65Cu. Las masas nuclídicas de las dos especies son 62,929 y 64, 928, respectivamente. ¿Cuál es el porcentaje de los dos isótopos en una muestra de cobre cuyo peso atómico es 63,54?